Quando si parla di tumori cerebrali, i termini glioma e glioblastoma vengono spesso usati in modo intercambiabile, sebbene descrivano patologie con comportamento ed esiti molto diversi. Entrambi i tumori originano dalle cellule gliali, che sostengono e proteggono le cellule nervose nel cervello. Tuttavia, il glioblastoma rappresenta la forma più aggressiva e pericolosa per la vita all'interno del più ampio gruppo dei gliomi, e la sua diagnosi comporta implicazioni terapeutiche e prognostiche molto diverse.
Comprendere la distinzione tra glioma e glioblastoma è fondamentale per una diagnosi accurata, la pianificazione del trattamento, la valutazione della prognosi e la consulenza al paziente. Il tipo e il grado del tumore influenzano la velocità di crescita, il trattamento e le aspettative realistiche di pazienti e familiari.
Questo blog spiega la differenza tra glioma e glioblastoma in modo chiaro, strutturato e basato su evidenze scientifiche. Si avvale di conoscenze cliniche, dati sulla sopravvivenza e linee guida terapeutiche provenienti dai principali centri oncologici.
Glioma vs. glioblastoma: alla scoperta delle nozioni di base
Cos'è un glioma?
I tumori cerebrali vengono generalmente classificati in base al tipo di cellule da cui hanno origine, poiché questo determina il comportamento del tumore e il trattamento. Tra queste categorie, i gliomi costituiscono uno dei gruppi più numerosi e più frequentemente diagnosticati di tumori cerebrali primari negli adulti. Si sviluppano all'interno del cervello o del midollo spinale e rappresentano una percentuale significativa dei tumori del sistema nervoso centrale riscontrati nella pratica clinica.
Il termine glioma è un termine generico che si riferisce ai tumori che originano dalle cellule gliali, le cellule di supporto che contribuiscono al mantenimento della normale funzione cerebrale. Poiché le cellule gliali sono presenti in tutto il cervello e nel midollo spinale, i gliomi possono insorgere in diverse sedi e influenzare un'ampia gamma di funzioni neurologiche. È importante sottolineare che i gliomi non costituiscono un'unica entità patologica, bensì un gruppo eterogeneo di tumori che differiscono per origine cellulare, comportamento biologico e decorso clinico.
I gliomi variano notevolmente per velocità di crescita, aggressività e risposta al trattamento. Alcuni gliomi crescono lentamente e possono rimanere stabili per anni con sintomi minimi, mentre altri crescono rapidamente e invadono il tessuto cerebrale circostante. Questa ampia variabilità implica che gli approcci terapeutici e gli esiti possano differire significativamente da un paziente all'altro. Il grado del tumore, le caratteristiche molecolari e la localizzazione cerebrale giocano un ruolo cruciale nel determinare la prognosi e nell'orientare le decisioni cliniche.
Ci occupiamo della pianificazione
Concentrati sul recupero
Dall'assistenza per il visto medico al prelievo in aeroporto e al soggiorno in loco, HOSPIDIO gestisce l'intero viaggio per cure mediche.
Invia la tua richiesta di trattamento
Tipi di gliomi
I gliomi vengono ulteriormente classificati in base al tipo di cellule gliali a cui assomigliano maggiormente all'esame microscopico. Questa classificazione aiuta i medici a comprendere come è probabile che il tumore si comporti e quali trattamenti potrebbero essere più efficaci.
1. Astrocitomi:
Gli astrocitomi originano dagli astrociti, le cellule gliali a forma di stella che sostengono i neuroni e contribuiscono a regolare l'ambiente chimico del cervello. Questi tumori rappresentano il tipo più comune di glioma e possono manifestarsi a qualsiasi età. Gli astrocitomi variano da tumori a crescita lenta e di basso grado a forme altamente aggressive. Il glioblastoma è un astrocitoma di grado 4, che rappresenta la forma più grave di questa categoria.
2. Oligodendrogliomi:
Gli oligodendrogliomi si sviluppano dagli oligodendrociti, le cellule gliali responsabili della produzione di mielina, la guaina protettiva che riveste le fibre nervose. Questi tumori tendono a crescere più lentamente degli astrocitomi e sono spesso associati a una migliore risposta al trattamento e a una maggiore sopravvivenza.
3. Ependimomi:
Gli ependimomi originano dalle cellule ependimali, che rivestono i ventricoli cerebrali e il canale centrale del midollo spinale. Questi tumori possono colpire sia bambini che adulti e possono interferire con il normale flusso del liquido cerebrospinale, causando un aumento della pressione intracranica. Il loro comportamento varia a seconda della localizzazione e del grado di malignità.
Questa classificazione basata sulle cellule fornisce le basi per comprendere le differenze biologiche tra i gliomi e mette in luce il motivo per cui il trattamento e la prognosi possono variare notevolmente da paziente a paziente.
Gradi del glioma
Secondo l'Organizzazione Mondiale della Sanità (OMSI gliomi vengono classificati in base al grado di anomalia che le cellule tumorali presentano al microscopio.
| Classificazione OMS | Comportamento del tumore | Personaggi chiave | Implicazioni cliniche |
| Grade 1 | Crescita lenta | Spesso ben definito, non invasivo, quasi benigno | Spesso trattato con il solo intervento chirurgico; la sopravvivenza a lungo termine è frequente. |
| Grade 2 | Di basso grado ma infiltrante | Cresce lentamente ma si diffonde al tessuto cerebrale circostante. | Richiede un monitoraggio a lungo termine del rischio di progressione verso gradi superiori |
| Grade 3 | Maligno e a rapida crescita | Cellule anomale con rapida divisione cellulare | Necessita di un trattamento combinato con chirurgia, radioterapia e chemioterapia. |
| Grade 4 | Altamente maligno | Crescita rapida, invasione dei tessuti e aree di necrosi | Il glioblastoma rientra esclusivamente nel grado 4 e richiede un trattamento aggressivo. |
Che cos'è un glioblastoma?
Il glioblastoma, noto anche come glioblastoma multiforme, è il tumore cerebrale primario più aggressivo e letale negli adulti. Rappresenta una quota considerevole dei tumori cerebrali maligni diagnosticati in tutto il mondo ed è noto per la sua rapida progressione e la prognosi infausta. A differenza di molti altri tumori cerebrali, il glioblastoma cresce rapidamente e si diffonde al tessuto cerebrale circostante, rendendo estremamente difficile la sua completa rimozione chirurgica. Il glioblastoma non costituisce una categoria di malattia a sé stante, bensì la forma più aggressiva all'interno dello spettro degli astrocitomi.
Secondo il sistema di classificazione dei tumori cerebrali dell'OMS, il glioblastoma è classificato come glioma astrocitico di grado 4. Questa classificazione riflette la sua elevata malignità, caratterizzata da una crescita cellulare incontrollata, un'estesa invasione delle strutture cerebrali circostanti e aree di necrosi delle cellule tumorali dovute a un insufficiente apporto di sangue. Una delle caratteristiche distintive del glioblastoma è la sua resistenza al trattamento. Anche con terapie aggressive che includono chirurgia, radioterapia e chemioterapia, il tumore recidiva frequentemente. La sua capacità di infiltrarsi nel tessuto cerebrale sano a livello microscopico permette alle cellule cancerose di persistere anche dopo il trattamento, contribuendo agli elevati tassi di recidiva. Queste caratteristiche biologiche rendono il glioblastoma uno dei tumori cerebrali più difficili da gestire nella pratica clinica e sottolineano la necessità di una continua ricerca di terapie più efficaci.
Caratteristiche biologiche del glioblastoma
Il glioblastoma è definito da diverse caratteristiche biologiche distinte che ne spiegano il comportamento aggressivo e la scarsa risposta al trattamento.
- Divisione cellulare rapidaLe cellule del glioblastoma si dividono a una velocità molto elevata, il che porta a una rapida crescita del tumore e a un rapido peggioramento dei sintomi. Questa rapida proliferazione consente al tumore di aumentare di dimensioni in un breve periodo di tempo, causando spesso un improvviso declino neurologico.
- Aree di necrosiPoiché il tumore cresce più velocemente di quanto il suo apporto di sangue possa supportare, alcune sue parti vengono private di ossigeno e nutrienti. Ciò provoca aree di necrosi, ovvero tessuto morto, che rappresentano una caratteristica distintiva riscontrabile nelle immagini diagnostiche e nell'esame istologico del glioblastoma. La necrosi è uno dei motivi principali per cui il glioblastoma viene classificato come tumore di grado 4.
- Formazione estesa di vasi sanguigniI glioblastomi stimolano la formazione di nuovi vasi sanguigni, un processo noto come angiogenesi. Questi vasi sanguigni anomali forniscono nutrienti al tumore e ne supportano la rapida crescita. Tuttavia, sono spesso mal strutturati, il che contribuisce al gonfiore e alla fuoriuscita di liquidi nel tessuto cerebrale circostante.
- Infiltrazione nel tessuto cerebrale circostanteA differenza dei tumori che crescono come una singola massa, le cellule del glioblastoma si diffondono a livello microscopico nel tessuto cerebrale sano circostante. Questa modalità di crescita infiltrativa rende la rimozione chirurgica completa quasi impossibile ed è una delle principali cause di recidiva del tumore dopo il trattamento.
Nel loro insieme, queste caratteristiche spiegano perché il glioblastoma si comporta in modo più aggressivo rispetto ad altri gliomi e perché richiede approcci terapeutici intensivi e multimodali.
Glioma vs Glioblastoma: Tabella delle principali differenze
| Caratteristica | Glioma | glioblastoma |
| Definizione | Gruppo di tumore derivante da cellule gliali | Il glioma di grado 4 più aggressivo |
| Grado del tumore | Grado 1 a Grado 4 | Sempre di livello 4 |
| Velocità di crescita | Da lento a veloce | Molto veloce |
| Invasività | Forse localizzato | Altamente infiltrante |
| Rimozione chirurgica | Spesso possibile nei gradi inferiori | Raramente completo |
| Rischio di recidiva | Dipende dal grado | Molto alto |
| Sopravvivenza media | Anni di tumori di basso grado | mesi 12-15 |
| Trattamento standard | Intervento chirurgico +/- radioterapia +/- chemioterapia | Chirurgia + radioterapia + chemioterapia |
| Prognosi | Ampia gamma, spesso con gradazioni basse favorevoli | Nel complesso scarso |
Il glioma è un termine generico che comprende diversi tipi di tumori cerebrali con gradi, velocità di crescita ed esiti variabili. Alcuni gliomi crescono lentamente e spesso possono essere gestiti efficacemente, soprattutto nei gradi più bassi. Al contrario, il glioblastoma rappresenta l'estremità più aggressiva dello spettro dei gliomi. È sempre un tumore di grado 4, cresce molto rapidamente, invade il tessuto cerebrale circostante, presenta un alto rischio di recidiva e richiede un trattamento intensivo e combinato. Di conseguenza, la prognosi per il glioblastoma è significativamente peggiore rispetto alla maggior parte degli altri gliomi.
Sintomi del glioma e del glioblastoma: segni simili, velocità di progressione diversa
I sintomi del glioma e del glioblastoma variano a seconda della localizzazione del tumore nel cervello, delle sue dimensioni e della sua velocità di crescita. Poiché diverse aree del cervello controllano funzioni diverse, anche tumori di piccole dimensioni possono causare sintomi evidenti se interessano zone critiche. In generale, entrambe le patologie condividono molti sintomi, ma la velocità con cui questi si sviluppano e peggiorano spesso è differente.
Sintomi comuni in entrambe le condizioni
- Mal di testa persistenti
- Convulsioni
- Debolezza su un lato del corpo
- Cambiamenti nel linguaggio o nella vista
- problemi di memoria
Differenze nella progressione dei sintomi
- Glioma: I sintomi spesso si sviluppano gradualmente e possono peggiorare lentamente nel corso di mesi o addirittura anni, soprattutto nei tumori di basso grado. Inizialmente, i pazienti potrebbero ignorare i cambiamenti più lievi, il che porta a una diagnosi tardiva.
- Glioblastoma: I sintomi tendono a progredire rapidamente, a volte nell'arco di poche settimane. Un improvviso declino neurologico, forti mal di testa o l'insorgenza di nuove crisi epilettiche sono comuni e spesso richiedono una valutazione medica urgente.
Questa rapida progressione dei sintomi è una caratteristica clinica fondamentale del glioblastoma e spesso porta a una diagnosi precoce, anche se la malattia stessa è già in stadio avanzato al momento dell'individuazione.
Diagnosi: come i medici distinguono tra glioma e glioblastoma
La distinzione tra glioma e glioblastoma è fondamentale per pianificare il trattamento più appropriato e comprendere il decorso previsto della malattia. I medici seguono un processo diagnostico strutturato e graduale che combina tecniche di imaging avanzate, esame istologico e test molecolari. Ogni fase contribuisce in modo significativo a chiarire l'aggressività del tumore e a definire il trattamento più indicato.
1. Diagnostica per immagini del cervello (risonanza magnetica con mezzo di contrasto)
Il percorso diagnostico inizia solitamente con una risonanza magnetica con mezzo di contrasto, che fornisce immagini dettagliate del cervello e aiuta i medici a valutare le dimensioni, la posizione e il comportamento del tumore.
- Il glioblastoma si presenta spesso come una massa irregolare e dall'aspetto aggressivo. Tipicamente mostra un enhancement disomogeneo del contrasto, un significativo edema cerebrale circostante e aree centrali scure che rappresentano tessuto morto o necrotico. Queste caratteristiche suggeriscono una rapida crescita e infiltrazione nel tessuto cerebrale circostante.
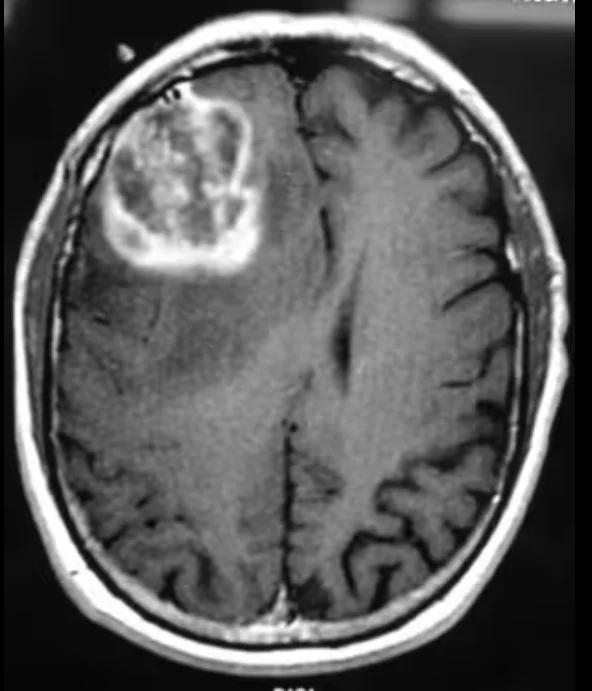
- I gliomi di grado inferiore, d'altro canto, appaiono solitamente più uniformi e ben definiti. Tendono a crescere più lentamente, causano meno gonfiore e spesso non presentano aree di necrosi tissutale. Alcuni potrebbero non mostrare alcun enhancement significativo con il mezzo di contrasto.
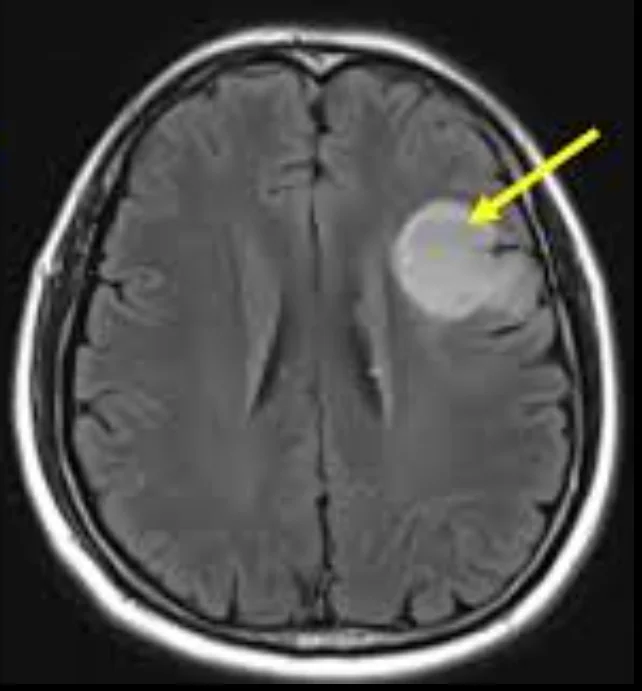
Sebbene la risonanza magnetica fornisca indizi importanti, le sole immagini diagnostiche non possono confermare l'esatto tipo o grado del tumore.
2. Biopsia o esame del tessuto chirurgico
Per formulare una diagnosi definitiva, i medici devono esaminare il tessuto tumorale vero e proprio.
- Ciò avviene tramite una biopsia stereotassica (una procedura minimamente invasiva) oppure durante la rimozione chirurgica del tumore, se l'intervento chirurgico è fattibile.
- Un neuropatologo studia il tessuto al microscopio per valutare l'aspetto delle cellule, i modelli di crescita e i segni di aggressività, come la rapida divisione cellulare o la necrosi.
Questo passaggio è essenziale per determinare se il tumore è un glioma di basso grado o un glioblastoma di grado 4, che è la forma più aggressiva di glioma.
3. Test molecolari e genetici
La moderna diagnosi dei tumori cerebrali va oltre ciò che è visibile al microscopio. I medici ora eseguono test molecolari sul tessuto tumorale per classificare meglio la malattia e personalizzare il trattamento.
I principali indicatori includono:
- Stato di mutazione IDH: i tumori con mutazione IDH generalmente crescono più lentamente e sono associati a una prognosi migliore. I glioblastomi sono spesso di tipo IDH wild type, ovvero privi di questa mutazione.
- Metilazione del promotore di MGMT: questo marcatore aiuta a prevedere la risposta del tumore alla chemioterapia, in particolare alla temozolomide. I pazienti con tumori con metilazione di MGMT spesso presentano una migliore risposta al trattamento.
Queste caratteristiche molecolari non solo confermano la diagnosi, ma svolgono anche un ruolo fondamentale nella scelta delle opzioni terapeutiche e nella stima dei risultati.
Ci occupiamo della pianificazione
Concentrati sul recupero
Dall'assistenza per il visto medico al prelievo in aeroporto e al soggiorno in loco, HOSPIDIO gestisce l'intero viaggio per cure mediche.
Invia la tua richiesta di trattamento
Perché è importante una diagnosi accurata
Capire se un tumore è un glioma o un glioblastoma aiuta i medici a: scegliere il piano di trattamento più efficace, stimare la prognosi con maggiore precisione, evitare trattamenti eccessivi o insufficienti e fornire a pazienti e famiglie aspettative più chiare. Una diagnosi precisa garantisce che ogni paziente riceva cure personalizzate in base alla biologia del tumore, non solo al suo aspetto.
Trattamento del glioma
Il trattamento del glioma è guidato dal grado del tumore, dal profilo molecolare, dalle dimensioni, dalla localizzazione e dallo stato di salute generale del paziente. Poiché i gliomi presentano un comportamento molto variabile, i piani di trattamento sono individualizzati anziché standardizzati.
Chirurgia
La rimozione chirurgica massimale possibile in sicurezza è solitamente il primo passo del trattamento, quando possibile. L'obiettivo è rimuovere la maggior parte del tumore senza danneggiare aree cerebrali vitali.
- La chirurgia è più efficace nei gliomi di basso grado, dove i tumori sono più localizzati
- La rimozione del tessuto tumorale riduce la pressione all'interno del cervello.
- Molti pazienti riscontrano un miglioramento di sintomi come mal di testa o debolezza dopo l'intervento chirurgico.
Radioterapia
La radioterapia viene utilizzata per distruggere le cellule tumorali residue dopo l'intervento chirurgico o quando l'intervento chirurgico non è completamente fattibile. La radioterapia è generalmente raccomandata quando:
- Il tumore è di grado 3 o superiore
- Dopo l'intervento chirurgico persiste un tumore residuo.
- Il tumore mostra segni di progressione
Chemioterapia
La chemioterapia viene spesso combinata con la radioterapia o utilizzata da sola, a seconda del tipo e del grado del tumore. Gli approcci chemioterapici più comuni includono:
- La temozolomide è ampiamente utilizzata per i gliomi di grado più elevato.
- La chemioterapia PCV (procarbazina, lomustina e vincristina) è particolarmente efficace in alcuni oligodendrogliomi.
In alcuni casi, i gliomi di basso grado con caratteristiche favorevoli possono essere monitorati attentamente con esami di imaging regolari prima di iniziare la radioterapia o la chemioterapia, consentendo ai pazienti di ritardare gli effetti collaterali correlati al trattamento mantenendo al contempo il controllo della malattia.
Trattamento del glioblastoma
Il trattamento del glioblastoma è urgente e richiede un coordinamento accurato, poiché questo tumore cresce rapidamente e tende a diffondersi al tessuto cerebrale circostante. La gestione del caso è affidata a un team medico multidisciplinare, che in genere comprende neurochirurghi, radioterapisti, oncologi medici, neurologi, specialisti della riabilitazione e professionisti delle cure palliative. Poiché il glioblastoma non può essere curato con una singola terapia, il trattamento si basa su un approccio combinato e graduale, volto a controllare la crescita del tumore, alleviare i sintomi e preservare la qualità della vita il più a lungo possibile.
1. Rimozione chirurgica sicura massima
Il trattamento di solito inizia con un intervento chirurgico massimale sicuro, il che significa che i chirurghi rimuovono la maggior parte possibile del tumore preservando le funzioni cerebrali vitali come il linguaggio, il movimento, la vista e la memoria.
L'intervento chirurgico aiuta a:
- Ridurre la pressione all'interno del cervello
- Migliora i sintomi neurologici come mal di testa, convulsioni o debolezza.
- Fornire tessuto per una diagnosi accurata e per i test molecolari.
- Migliorare l'efficacia dei trattamenti di follow-up
- Poiché le cellule del glioblastoma spesso infiltrano il tessuto cerebrale sano, la rimozione completa è raramente possibile.
Anche dopo interventi chirurgici estesi, le cellule tumorali microscopiche rimangono quasi sempre.
2. Radioterapia con chemioterapia concomitante
Dopo l'intervento chirurgico, la maggior parte dei pazienti riceve radioterapia combinata con chemioterapia, che di solito inizia entro poche settimane.
- La radioterapia si concentra sul letto tumorale e sulle aree circostanti in cui possono essere presenti cellule cancerose microscopiche. In genere viene somministrata cinque giorni a settimana per circa sei settimane.
- La chemioterapia (più comunemente temozolomide per via orale) viene somministrata insieme alla radioterapia per rendere le cellule tumorali più sensibili ai danni da radiazioni.
Questo approccio combinato è considerato lo standard di cura e migliora significativamente la sopravvivenza rispetto alla sola radioterapia.
3. Chemioterapia di mantenimento (adiuvante)
Una volta completata la radioterapia, i pazienti di solito proseguono con la chemioterapia di mantenimento.
- La temozolomide viene assunta a cicli per diversi mesi
- L'obiettivo è rallentare la ricrescita del tumore e prolungare il controllo della malattia.
- La tolleranza e la risposta vengono monitorate attentamente mediante scansioni e analisi del sangue periodiche.
La durata della terapia di mantenimento dipende dalla risposta del paziente, dal suo stato di salute generale e dal profilo degli effetti collaterali.
4. Opzioni di trattamento aggiuntive e avanzate
In alcuni pazienti selezionati, possono essere raccomandate terapie aggiuntive:
- Campi di trattamento tumorale (TTF): un dispositivo indossabile che eroga campi elettrici a bassa intensità per interrompere la divisione delle cellule tumorali. Può contribuire a prolungare la sopravvivenza se utilizzato con costanza in combinazione con la chemioterapia.
- Sperimentazioni cliniche: i pazienti possono essere idonei a partecipare a sperimentazioni cliniche che prevedono terapie mirate, immunoterapia, vaccini o nuove combinazioni di farmaci.
Questi studi clinici offrono accesso a trattamenti emergenti non ancora ampiamente disponibili. L'idoneità dipende dalla biologia del tumore, dai trattamenti precedenti e dallo stato di salute generale.
5. Cure di supporto, riabilitazione e gestione dei sintomi
Le cure di supporto sono una parte fondamentale del trattamento del glioblastoma e proseguono per tutta la durata della malattia.
Questo può includere:
- Farmaci per convulsioni, edema cerebrale, dolore o affaticamento
- Fisioterapia, terapia occupazionale e logopedia per il recupero funzionale.
- Supporto nutrizionale e consulenza psicologica
- Cure palliative per migliorare il comfort, l'indipendenza e il benessere emotivo.
L'integrazione precoce di cure di supporto aiuta i pazienti a mantenere una migliore qualità della vita durante i trattamenti intensivi.
Tassi di sopravvivenza nel glioma rispetto al glioblastoma: cosa mostrano gli studi
Per quanto riguarda la sopravvivenza al glioblastoma, la ricerca clinica dimostra costantemente che gli esiti rimangono sfavorevoli anche con i trattamenti attuali, sebbene nel tempo si siano registrati modesti miglioramenti.
Secondo PubMLa sopravvivenza globale mediana per gli adulti con glioblastoma di nuova diagnosi è in genere di circa 12-15 mesi, anche con la massima chirurgia possibile seguita da radioterapia e chemioterapia. Questo dato è supportato da revisioni sistematiche e ampi studi istituzionali che dimostrano come il trattamento standard combinato migliori la sopravvivenza rispetto alla sola radioterapia.
Un'analisi sistematica degli esiti del glioblastoma ha riportato una sopravvivenza globale mediana di circa 13.5 mesi, con tassi di sopravvivenza a cinque anni generalmente inferiori al 6%. Un altro PubMed Lo studio ha riportato risultati con una sopravvivenza mediana compresa tra 9 e 14 mesi, a seconda dell'intensità del trattamento e dei fattori relativi al paziente.
La probabilità di sopravvivenza varia notevolmente in base a diversi fattori chiave:
- Estensione della resezione chirurgica: I pazienti sottoposti a una rimozione più completa del tumore tendono a vivere più a lungo rispetto a quelli che si sottopongono solo a una biopsia.
- Marcatori molecolari: I tumori con metilazione del promotore MGMT e mutazioni IDH sono associati a una sopravvivenza più lunga rispetto ai tumori privi di questi marcatori.
- Età e salute generale: I pazienti più giovani spesso ottengono risultati migliori rispetto ai pazienti più anziani.
Anche con un trattamento ottimale, la sopravvivenza a lungo termine è rara. I tassi di sopravvivenza a cinque anni nelle popolazioni contemporanee sono generalmente bassi, spesso a una sola cifra, a testimonianza dell'aggressività biologica del glioblastoma. Alcune revisioni sistematiche meno recenti suggeriscono una sopravvivenza a cinque anni intorno al 4% in molte coorti, e meno dell'1% potrebbe sopravvivere per dieci anni o più.
Al contrario, i gliomi di grado inferiore (grado 2 e 3) presentano in genere una sopravvivenza molto più lunga, spesso di anni o decenni in molti pazienti, soprattutto quando le caratteristiche molecolari e la risposta al trattamento sono favorevoli. Nel complesso, sebbene la sopravvivenza mediana per il glioblastoma si mantenga intorno ai 12-15 mesi, gli esiti individuali variano notevolmente in base a fattori biologici, clinici e correlati al trattamento.
Perché il glioblastoma recidiva frequentemente?
Nonostante le terapie aggressive che includono chirurgia, radioterapia e chemioterapia, la recidiva del glioblastoma è frequente e spesso inevitabile. La maggior parte dei pazienti sperimenta una ricrescita del tumore, anche quando il trattamento segue i migliori standard disponibili. Una delle ragioni principali è la diffusione microscopica dei tumori oltre i margini visibili. Le cellule del glioblastoma infiltrano il tessuto cerebrale circostante a livello microscopico, estendendosi ben oltre ciò che può essere visto con la risonanza magnetica o rimosso durante l'intervento chirurgico. Di conseguenza, le cellule tumorali spesso rimangono anche dopo la massima resezione possibile. Un altro fattore che contribuisce a questo fenomeno è la resistenza alla chemioterapia.
Le cellule del glioblastoma possono adattarsi e sviluppare resistenza a farmaci come la temozolomide, riducendo l'efficacia a lungo termine del trattamento. Alcune cellule tumorali sopravvivono alla terapia iniziale e in seguito favoriscono la ricrescita del tumore. Anche la limitata penetrazione dei farmaci attraverso la barriera emato-encefalica gioca un ruolo significativo. La barriera emato-encefalica protegge il cervello da sostanze nocive, ma impedisce anche a molti farmaci chemioterapici di raggiungere le cellule tumorali in concentrazioni adeguate, limitando l'impatto del trattamento.
A causa di questi fattori, la maggior parte delle recidive di glioblastoma si verifica entro un anno dal trattamento iniziale. La recidiva è solitamente più difficile da trattare e spesso richiede terapie aggiuntive, studi clinici o approcci di supporto.
Differenze tra glioma e glioblastoma in età pediatrica e adulta.
- Comportamento del tumore: Nei bambini, i gliomi sono spesso diversi da quelli degli adulti. Alcuni gliomi pediatrici crescono più lentamente e rispondono meglio al trattamento, mentre altri possono comunque essere aggressivi. Gli adulti hanno maggiori probabilità di sviluppare il glioblastoma, un tumore aggressivo a crescita rapida.
- Tolleranza al trattamento: Il corpo e il cervello dei bambini sono ancora in fase di sviluppo, quindi possono reagire in modo diverso a interventi chirurgici, chemioterapia o radioterapia. I medici valutano attentamente l'efficacia del trattamento, cercando al contempo di minimizzare gli effetti collaterali a lungo termine sulla crescita e sullo sviluppo cerebrale. Gli adulti possono manifestare maggiori effetti collaterali a seguito di trattamenti aggressivi e il recupero può essere più lento.
- Sintomi e diagnosi: Nei bambini, sintomi come cambiamenti nel rendimento scolastico, nel comportamento o nella coordinazione possono comparire per primi, a volte prima di evidenti segni fisici. Gli adulti spesso notano mal di testa, problemi di memoria o debolezza a un arto.
- Considerazioni a lungo termine: I pazienti pediatrici potrebbero necessitare di un monitoraggio continuo per valutare l'apprendimento, lo sviluppo e i cambiamenti cognitivi dopo il trattamento. Gli adulti potrebbero incontrare difficoltà nel tornare al lavoro o nel gestire le responsabilità quotidiane e potrebbero aver bisogno di supporto per la salute mentale e la qualità della vita.
Qualità della vita e cure di supporto
L'assistenza di supporto per i pazienti affetti da glioma o glioblastoma va oltre il trattamento del tumore stesso; l'obiettivo principale è aiutare i pazienti a rimanere il più possibile a proprio agio, indipendenti e attivi nella vita quotidiana. La gestione dei sintomi riveste un ruolo centrale, con farmaci personalizzati per controllare mal di testa, convulsioni, nausea, affaticamento e altri effetti collaterali, mentre la gestione del dolore è adattata alle esigenze di ciascun paziente. I servizi di riabilitazione, come la fisioterapia, la terapia occupazionale e la logopedia, contribuiscono a mantenere forza, mobilità, autonomia nelle attività quotidiane e capacità comunicative.
Il supporto emotivo e sociale è altrettanto importante: la consulenza psicologica, i gruppi di sostegno e l'orientamento per le famiglie aiutano i pazienti ad affrontare stress, ansia o depressione. I bambini potrebbero aver bisogno di ulteriore assistenza a scuola, nello sviluppo delle abilità sociali e in quello emotivo, mentre gli adulti potrebbero aver bisogno di aiuto per conciliare lavoro, responsabilità domestiche e mantenimento dell'indipendenza.
Si incoraggiano approcci olistici, tra cui alimentazione, esercizio fisico leggero e tecniche di rilassamento, per migliorare il benessere generale. Le cure palliative possono essere introdotte precocemente per migliorare il comfort, preservare la dignità e supportare sia i pazienti che le loro famiglie durante tutto il percorso terapeutico.
Leggi anche: Costo del trattamento dei tumori cerebrali in India
Prospettiva clinica
Dal punto di vista medico, il glioblastoma non è semplicemente una forma più grave di glioma, ma una malattia diversa e più aggressiva, con un proprio comportamento e specifiche sfide terapeutiche. A differenza dei gliomi di grado inferiore, i glioblastomi crescono più velocemente, colpiscono il cervello in modo più grave e sono più difficili da trattare. La diagnosi precoce tramite test molecolari (che analizzano il patrimonio genetico del tumore) è fondamentale perché aiuta i medici a scegliere i trattamenti più efficaci per ogni singolo paziente.
La cura di questi pazienti di solito coinvolge un team di specialisti, tra cui neurochirurghi, oncologi, radioterapisti, infermieri e terapisti. Lavorando insieme in questo modo, i medici possono migliorare i sintomi, rallentare la crescita del tumore e migliorare la qualità della vita sia dei pazienti affetti da glioma che da glioblastoma.
Conclusione: Glioma vs Glioblastoma
Il glioma è un'ampia categoria di tumori cerebrali che possono comportarsi in modo molto diverso a seconda del tipo e del grado. Alcuni gliomi crescono lentamente e possono rispondere bene al trattamento, mentre altri sono più aggressivi. Il glioblastoma, d'altra parte, è la forma più aggressiva di glioma. Cresce rapidamente, spesso recidiva dopo il trattamento e generalmente ha una prognosi di sopravvivenza più limitata. Distinguere chiaramente tra glioma e glioblastoma è fondamentale. Permette ai medici di scegliere i trattamenti più appropriati, aiuta i pazienti e le loro famiglie a capire cosa aspettarsi e consente a chi si prende cura di loro di pianificare efficacemente le cure di supporto.
Comprendendo queste differenze, pazienti, familiari e team sanitari possono prendere decisioni informate, prepararsi alle difficoltà e affrontare il trattamento con aspettative realistiche. Questa chiarezza non solo favorisce migliori risultati clinici, ma contribuisce anche a mantenere la qualità della vita e il benessere emotivo durante tutto il percorso.
Leggi altri blog correlati
Referenze
Blog recenti
Domande Frequenti
Il termine glioma si riferisce genericamente ai tumori cerebrali che originano dalle cellule gliali, le quali sostengono e proteggono le cellule nervose. I gliomi possono crescere lentamente o rapidamente e il loro grado di malignità varia da basso ad alto.
Il glioblastoma (GBM) è il tipo di glioma più aggressivo e di grado più elevato (grado IV). Cresce rapidamente, infiltra il tessuto cerebrale circostante e richiede un trattamento intensivo.
Sì. Il glioblastoma è un tipo di glioma, ma non tutti i gliomi sono glioblastomi.
Sì. Alcuni gliomi di basso o medio grado possono trasformarsi in glioblastoma nel tempo, soprattutto se non trattati o se geneticamente aggressivi.
Attualmente, il glioblastoma non è considerato curabile, ma il trattamento può: prolungare la sopravvivenza, ridurre i sintomi e migliorare la qualità della vita.
Il glioblastoma cresce rapidamente e può progredire nel giro di settimane o mesi, motivo per cui un trattamento tempestivo è essenziale.
La sopravvivenza varia, ma con il trattamento molti pazienti vivono dai 12 ai 18 mesi o anche di più, a seconda dell'età, dello stato di salute e della biologia del tumore.
Se l'intervento chirurgico non è possibile, si ricorre alla radioterapia e alla chemioterapia per controllare la crescita del tumore e gestire i sintomi.
Marcatori come la mutazione IDH e la metilazione MGMT aiutano a orientare le decisioni terapeutiche e a prevedere la risposta alla terapia.
Nella maggior parte dei casi non si tratta di una malattia ereditaria. Il glioblastoma si manifesta solitamente in forma sporadica, senza precedenti familiari.
Sanjana Sharma è un'educatrice certificata per il diabete con una solida formazione accademica in nutrizione e dietetica. Ha conseguito una laurea triennale in Nutrizione Clinica e Dietetica, una laurea magistrale in Alimentazione e Nutrizione presso la CCS University, un diploma in Salute e Educazione presso l'IGNOU e una certificazione NDEP. Dedicata ad aiutare i pazienti a gestire la propria salute attraverso cure e formazione personalizzate, Sanjana porta competenza e compassione nel suo lavoro. Oltre alla consulenza e alla scrittura, Sanjana ama tenersi aggiornata sulle tendenze della moda, condividere meme aziendali su Instagram e, naturalmente, pensare al cibo.
Dr. Manmohan Singh è un neurochirurgo di alto livello e vicepresidente del dipartimento di Neuroscienze presso Paras Health, Gurugram. Con oltre 25 anni di esperienza, è specializzato in interventi chirurgici complessi al cervello e alla colonna vertebrale, procedure alla base cranica e cure neurochirurgiche avanzate. In precedenza, ha ricoperto il ruolo di professore di neurochirurgia e direttore del Gamma Knife Centre presso l'AIIMS di Nuova Delhi, ed è ampiamente stimato per la sua eccellenza clinica e il suo approccio incentrato sul paziente.